伏欣奇拜单抗sJIA II期研究成果获《Rheumatology Ther》接收: 主要终点Day 28改良JIA ACR Pedi 30应答率实现94.1%,激素减停率达75%
发布时间
2026-03-02
阅读量
4545
分享
全身型幼年特发性关节炎(sJIA)是儿童风湿免疫领域极具挑战性的疾病之一。作为JIA的特殊亚型,sJIA并非典型的自身免疫性疾病,而是由固有免疫系统异常激活所驱动的自身炎症性疾病。其核心病理机制与IL-1β和IL-6等促炎因子的异常升高密切相关,临床表现包括弛张高热、皮疹、肝脾肿大及浆膜炎等。值得关注的是,约10%-30%的患儿可能并发巨噬细胞活化综合征(MAS),进展迅速且可危及生命。
近年来,靶向IL-1和IL-6通路的生物制剂显著改善了sJIA的治疗预后,使疾病管理进入精准靶向治疗时代。然而,在实际临床实践中,如何进一步提升治疗便利性、优化长期管理体验、提高治疗可及性,仍是当前亟待关注的重要方向。因此,围绕IL-1β通路开展更加便捷、安全、可持续的治疗方案探索,具有重要的临床价值与现实意义。因此,开发给药便捷、安全性优越且可及性高的IL-1β靶向药物,一直是临床未被满足的迫切需求。
在此背景下,由中国多家儿童风湿免疫中心共同完成的一项随机、开放标签、阳性对照的II期临床试验(NCT05925452)已获得国际期刊《Rheumatology and Therapy》正式接收。该研究系统评估了全人源抗IL-1β单克隆抗体伏欣奇拜单抗(Firsekibart )1在活动性sJIA患儿中的疗效与安全性。
一、研究设计
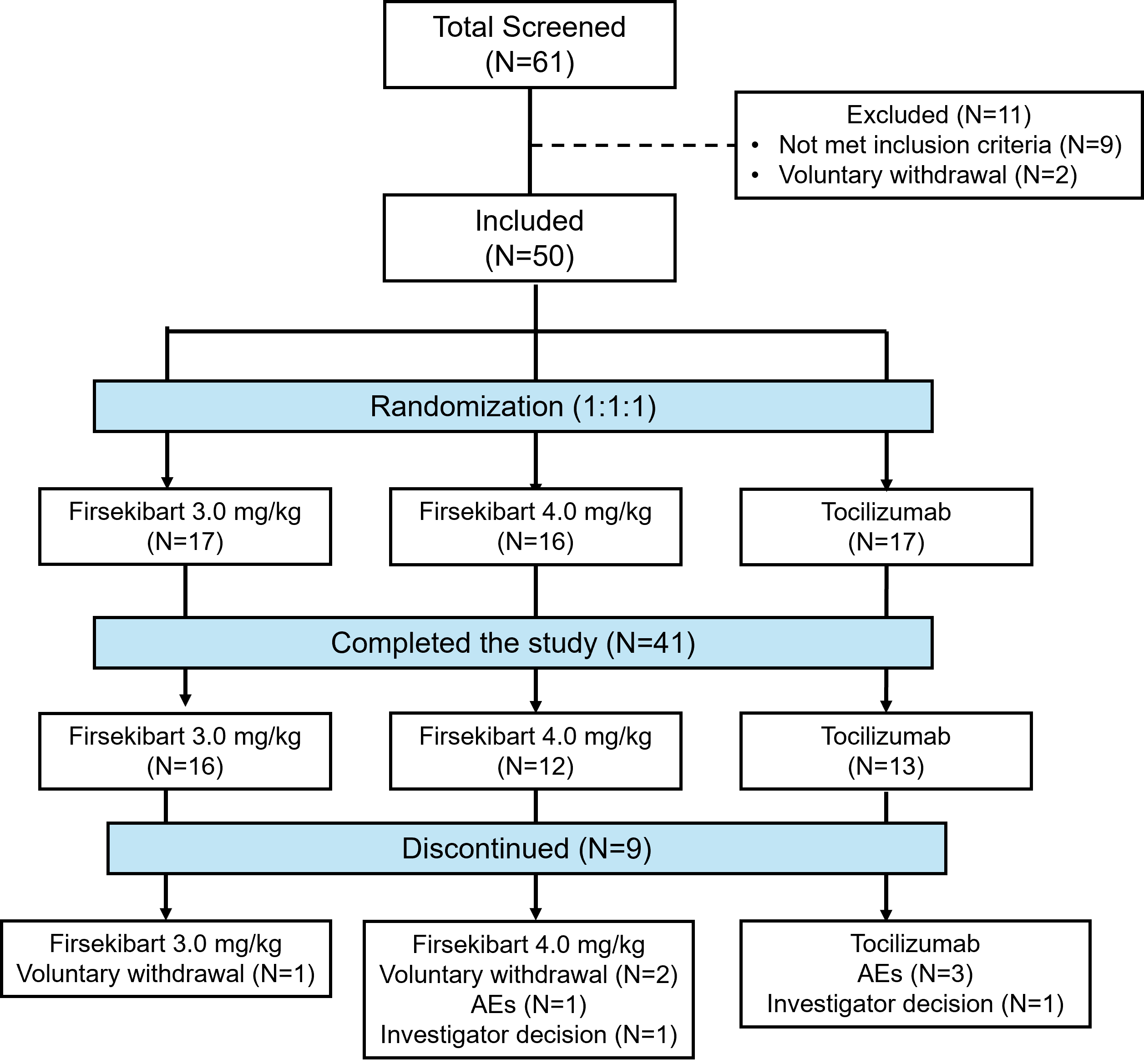
研究共纳入50例sJIA患儿,随机分配至伏欣奇拜单抗3.0 mg/kg组(17例)、4.0 mg/kg组(16例)或托珠单抗组(17例)。研究包括筛选期、导入治疗期(4周)、维持治疗期(20周)和随访期。共分为三个治疗组,分别为伏欣奇拜单抗3.0 mg/kg(每4周给药一次,皮下注射)、4.0 mg/kg每4周给药一次,皮下注射和托珠单抗组(每2周给药一次,静脉输注)。
研究D28达到ACR Pedi 30应答的受试者进入维持治疗期;未达到者结束治疗,进入随访期。
二、关键临床数据:疗效与安全性的双重认证
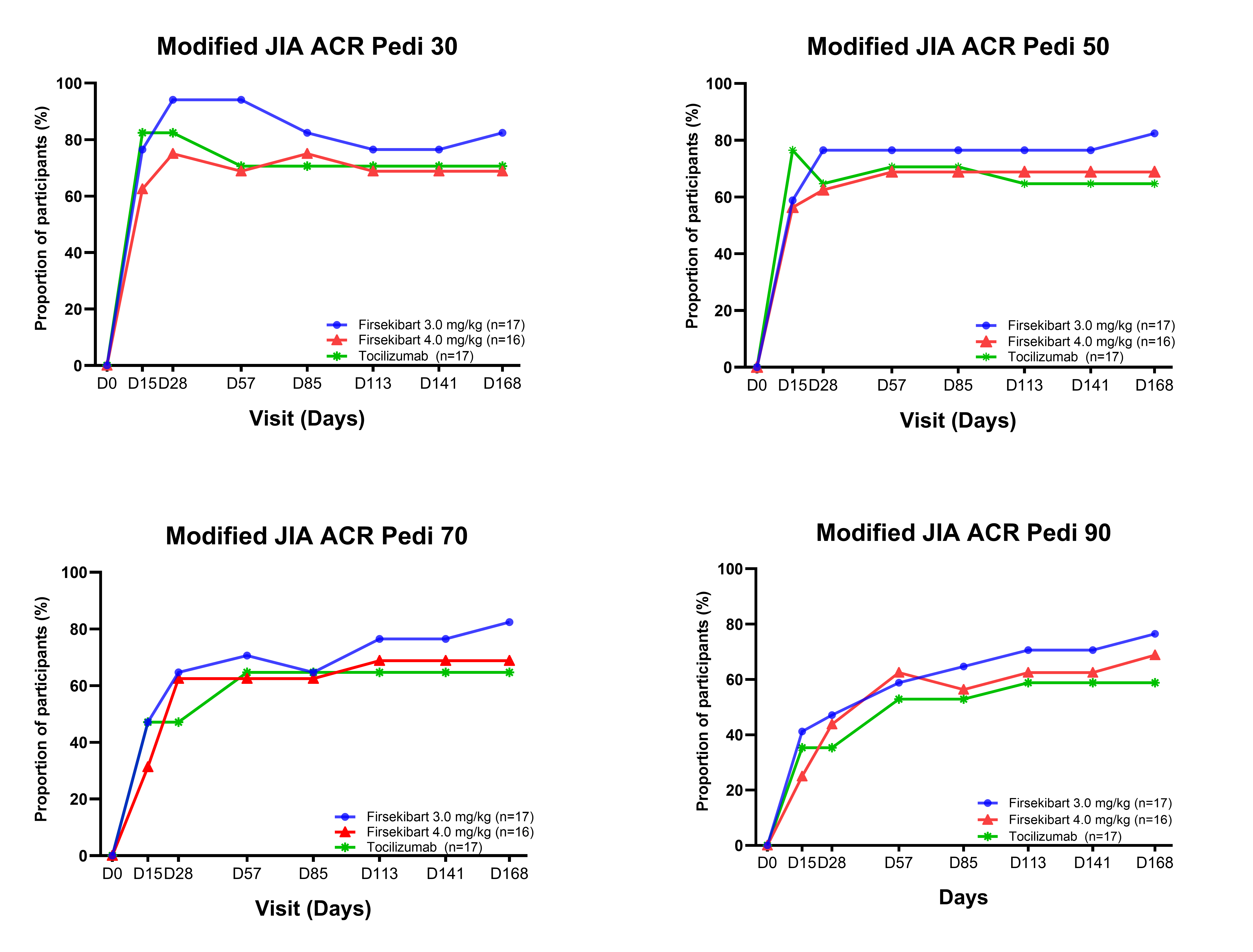
2.1 快速强效应答:Day 28 ACR Pedi 30 高达94.1%
在主要终点方面,伏欣奇拜单抗3.0 mg/kg组在第28天达到改良ACR Pedi 30应答率94.1%,为三组中最高。
其他IL-1/6i已公开数据
本研究阳性对照组(托珠单抗 ):82.4%
卡那单抗全球III期研究(第29天):82%2
阿那白滞素关键研究:67%3
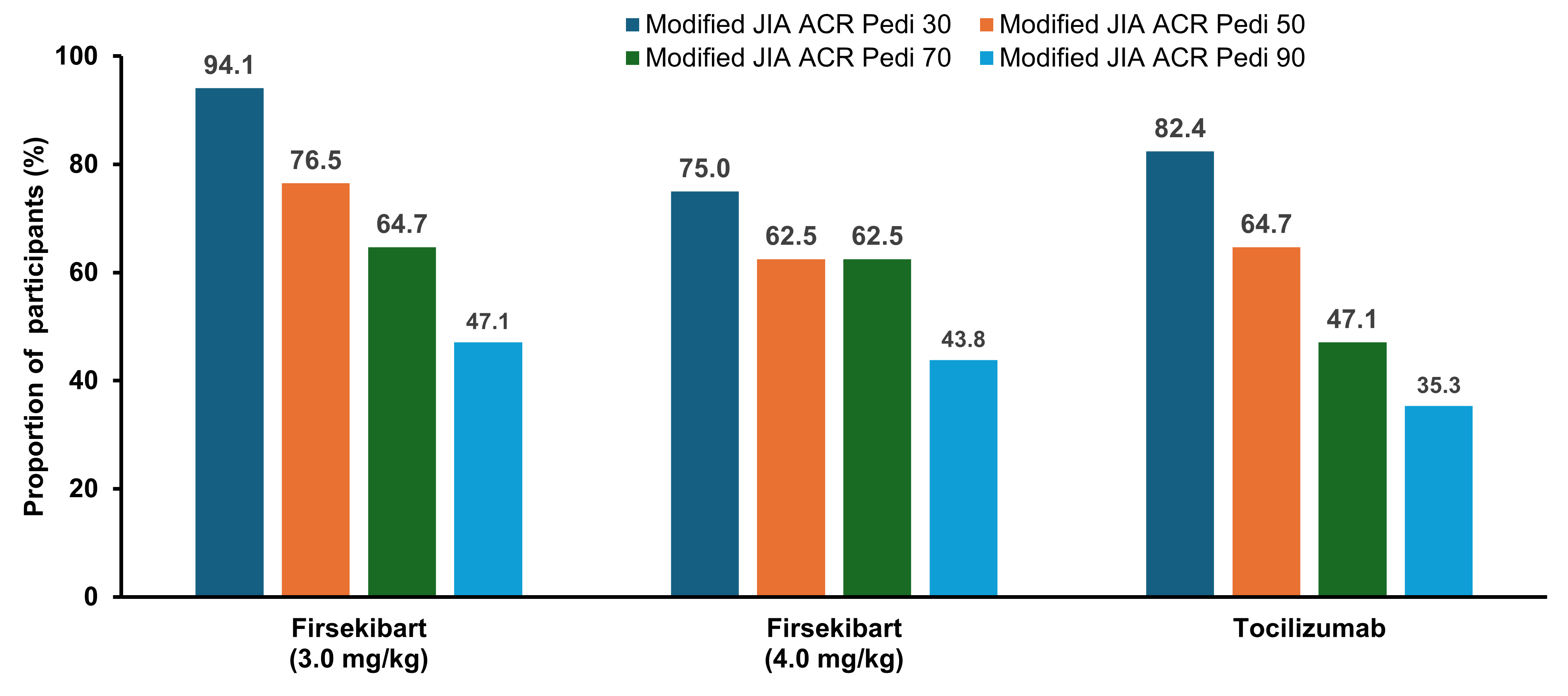
2.2 深度缓解优势: ACR Pedi 90 应答率达47.1%
伏欣奇拜单抗3.0 mg/kg组在ACR Pedi 50/70/90应答率分别为76.5%、64.7%和47.1%,托珠单抗组则分别为64.7%、47.1%和35.3%。在ACR Pedi 90这一更高标准的应答上,伏欣奇拜单抗组数值更高,提示其不仅能快速控制炎症,更能帮助患儿实现更深度的疾病缓解,这对于降低远期关节损伤风险至关重要。
2.3 激素喊停: 临床获益的硬终点
糖皮质激素减停是评估生物制剂“真实价值”的关键指标。至治疗结束时,伏欣奇拜单抗3.0 mg/kg组激素减停成功率高达75.0%,而4.0 mg/kg组和托珠单抗组分别为63.6%和62.5%。较高的激素减停比例提示,该方案在减少激素暴露方面具有积极意义,有助于降低长期使用糖皮质激素相关不良影响的风险。
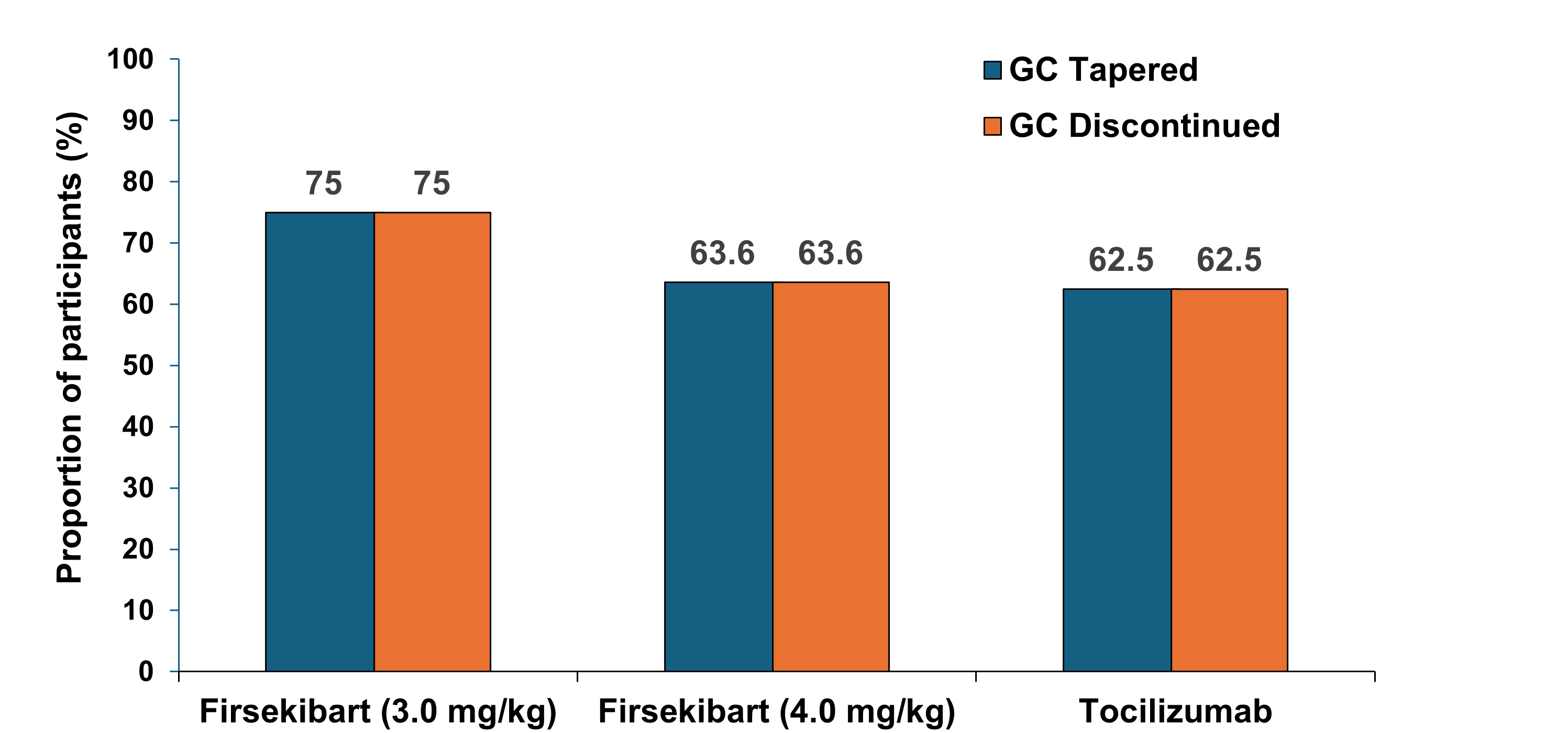
2.4 安全性“三零”记录
伏欣奇拜单抗3.0 mg/kg组在本研究中体现了较好的安全性;“三零”记录不仅降低了临床管理负担,更为药物的长期使用及适应症拓展提供了坚实保障
0 ≥3级治疗期间不良事件(TEAEs)
0 严重不良事件(SAEs)
0 巨噬细胞活化综合征(MAS)事件
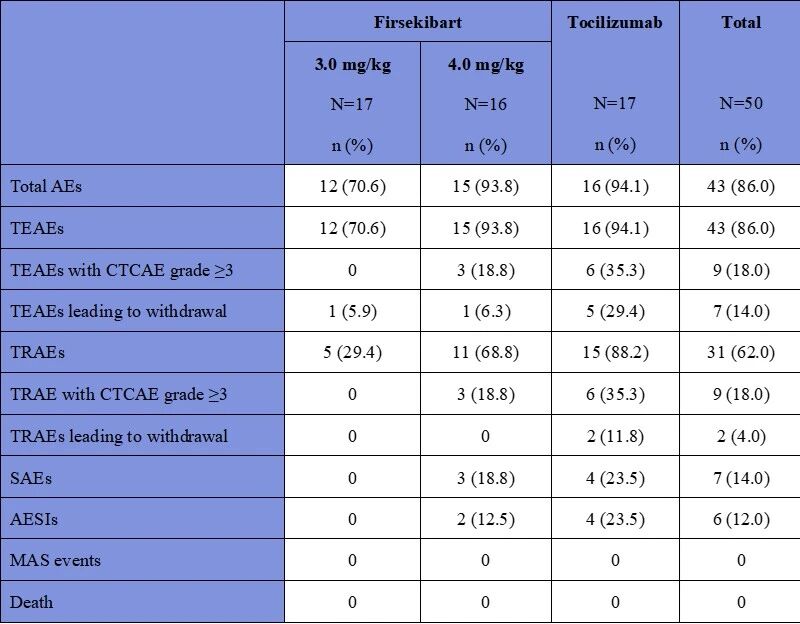
AE: 不良事件 AESI: 特别关注的不良事件 CTCAE: 不良事件通用术语标准 MAS: 巨噬细胞活化综合征 TEAE: 治疗中出现的不良事件 TRAE: 治疗相关不良事件
三、破局sJIA治疗“不可能金三角”:疗效、便捷、可及
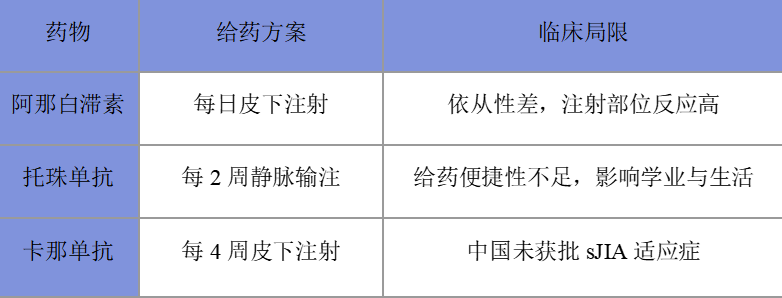
sJIA治疗长期面临结构性困境:高效、便捷、安全三者难以兼得。
伏欣奇拜单抗的三重破局
1. 疗效:94.1%的ACR Pedi 30应答率,47.1%的ACR Pedi 90深度缓解率。
2. 便捷:每4周一次皮下注射,极大解放患儿及家庭。
3. 可及:全人源抗体,有望成为中国首个可及的IL-1β单抗。
四、伏欣奇拜分子机制解码:四重设计如何转化为临床获益?
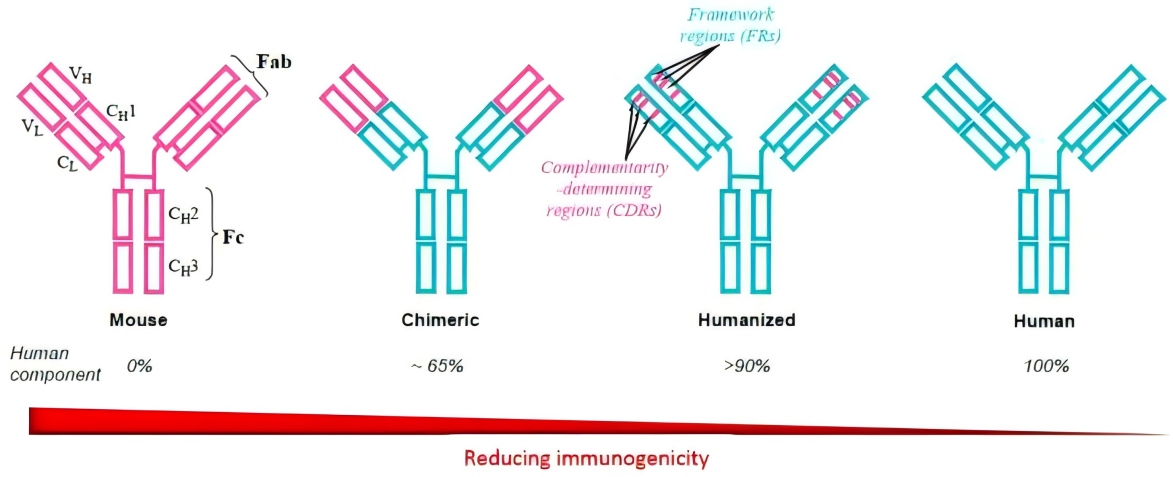
4.1 全人源抗体:免疫原性风险趋近于零6
免疫原性是影响生物制剂长期疗效和安全性的关键。从鼠源(ADA阳性率84%)到嵌合(40%)、人源化(9%),再到全人源(可低至0%),抗体人源化程度与免疫原性风险呈负相关。伏欣奇拜单抗采用全人源IgG4抗体,不含鼠源序列,临床验证的零ADA结果,从根源上降低了超敏反应及疗效衰减的风险。
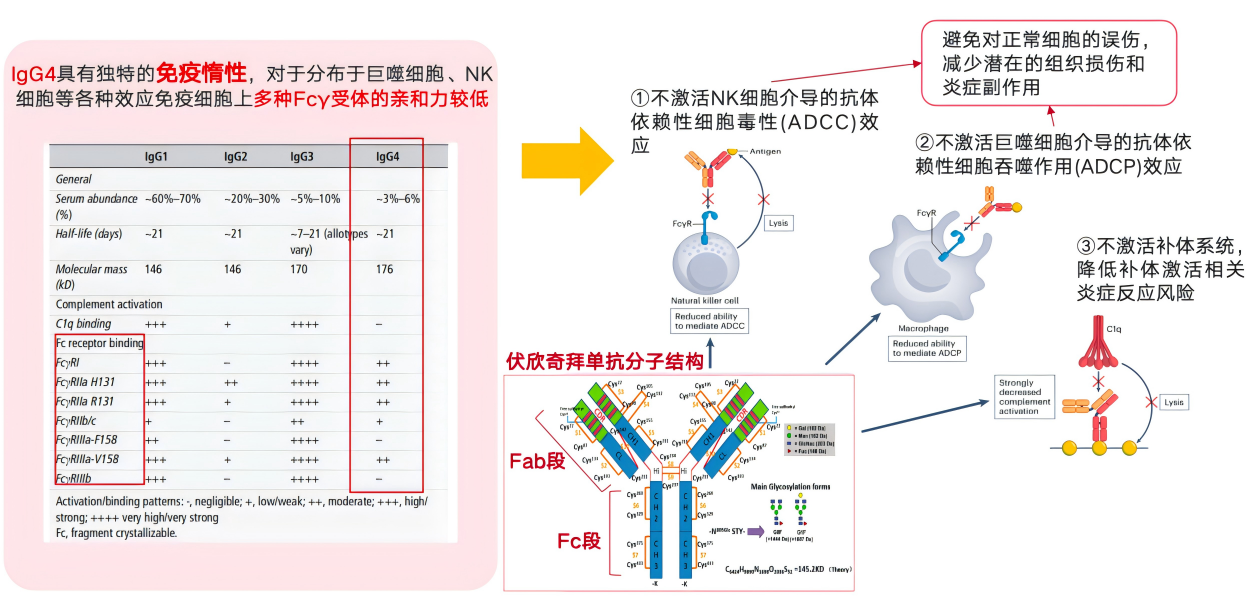
4.2 lgG4亚型:效应功能“沉默”提升安全性7-8
伏欣奇拜单抗采用独特的IgG4亚型,具备“效应功能沉默”特性:
不激活ADCC、ADCP效应,避免NK细胞/巨噬细胞介导的细胞毒性。
不激活补体系统,降低免疫复合物形成风险。这种设计使其在强效中和IL-1β的同时,减少非靶向的免疫激活,与临床观察到的优异安全性高度契合。
4.3 更低等电点(pl):延长半衰期,优化给药间隔7-8
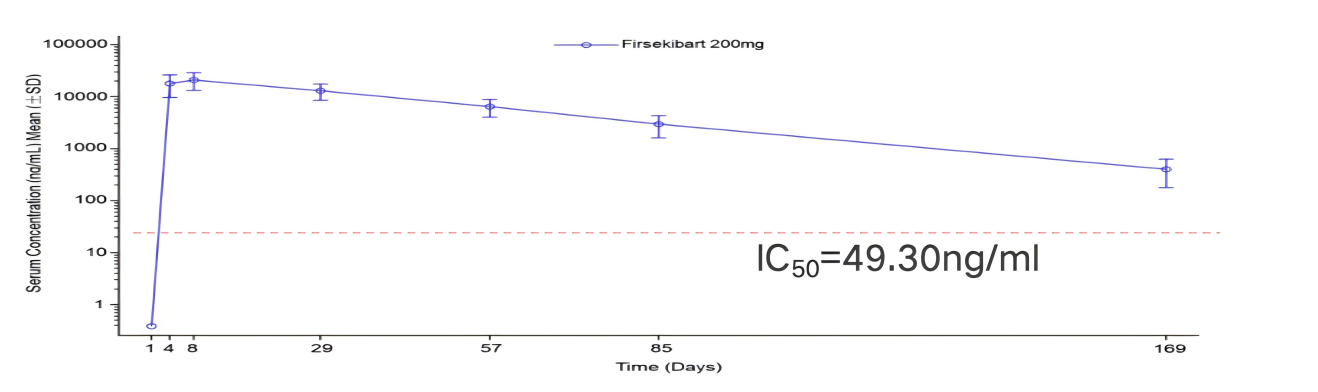
伏欣奇拜单抗的等电点(pI)为6.5–7.0,在生理pH下带负电荷(竞品多带正电荷,pI > 8.4)。药理学优势:负电荷特性可减缓药物在组织中的吸收和清除速率,延长半衰期。临床数据佐证:单次注射200mg后,169天仍可检出药物浓度,支持其每4周给药的便捷方案。
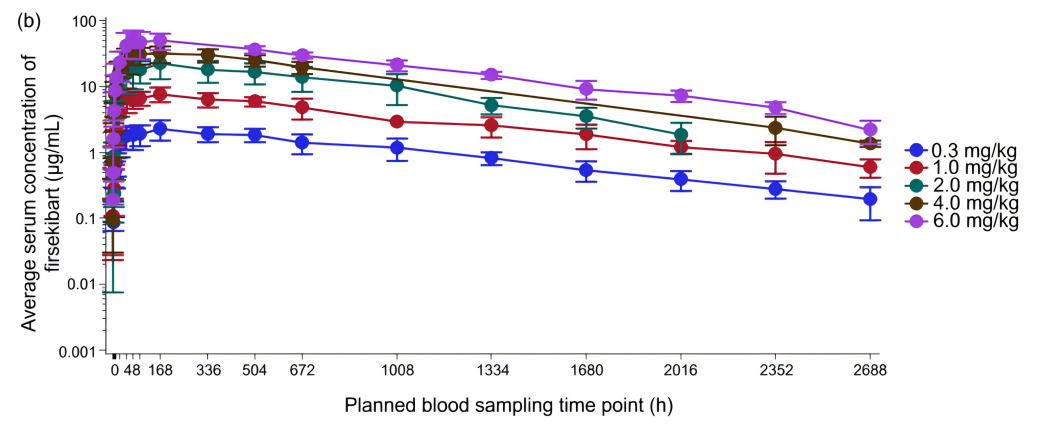
不同剂量伏欣奇拜单抗单次给药后的平均血药浓度-时间曲线图-半对数坐标 (从基线到第113天)
伏欣奇拜单抗 200 mg单次给药后的平均血药浓度-时间曲线图-半对数坐标 (从基线到第169天)
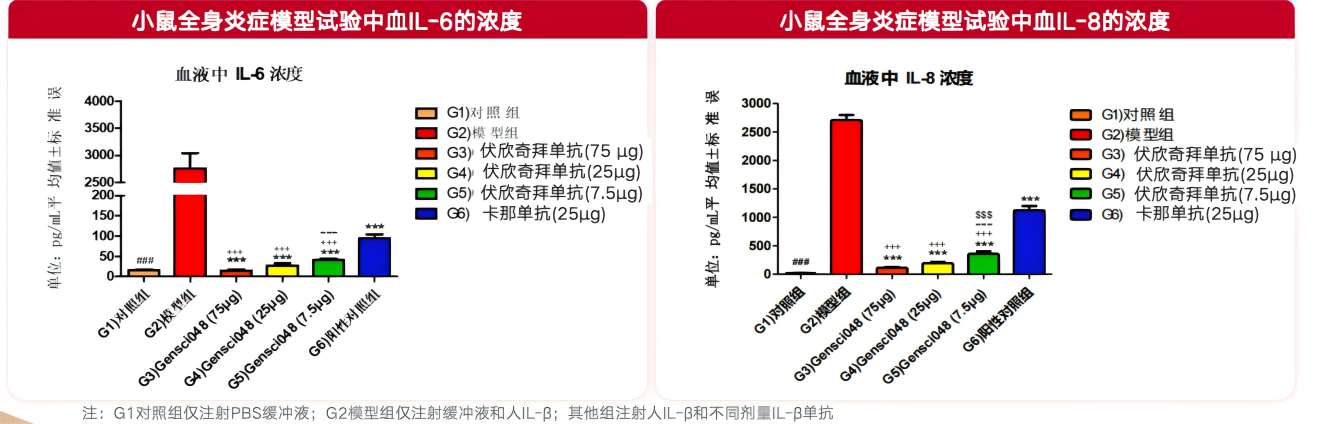
4.4 高亲和力结合:中和活性为同类5倍12
伏欣奇拜单抗对IL-1β的亲和力及中和活性约为同类产品的5倍。更强的阻断能力意味着在相同剂量下可实现更彻底的炎症通路抑制,为临床疗效提供坚实的药理学基础。
五、结语与展望
IL-1β是多种自身炎症性疾病的核心驱动因子,以下疾病存在IL-1β通路过度活化证据:
单基因自身炎症性疾病:CAPS、FMF、TRAPS、MKD、DIRA
多基因自身炎症性疾病:AOSD、复发性心包炎、MAS、Schnitzler综合征
炎症性关节病:其他JIA亚型、炎症性肠病相关关节炎
IL-1抑制剂获批
卡那单抗| IL-1β :CAPS、FMF/TRAPS/MKD、Still病(AOSD/sJIA)、痛风
阿那白滞素 | IL-1R:CAPS、DIRA、复发性心包炎
伏欣奇拜单抗在sJIA II期研究中展现的94.1%应答率、75%激素减停率、零严重事件安全性记录,不仅是数据的亮眼,更是其分子设计优势的临床验证。它不仅为sJIA患儿提供了一种兼具高效、长效、便捷的治疗新选择,更凭借全人源、IgG4亚型、低等电点等差异化壁垒,向更广泛的IL-1β介导的自身炎症性疾病矩阵研发。
参考文献:
1.Efficacy and Safety of Firsekibart in Treatment of Active Systemic Juvenile ldiopathic Arthritis: ARandomized Phase 2 Study. DOl:10.1007/s40744-026-00830-9
2.Ruperto N, et al. N Engl J Med. 2012,367(25):2396-406
3.Quartier P, et al. Ann Rheum Dis. 2011,70(5):747-54
4.Harding, et al. mAbs, 2(3), 256–265. https://doi.org/10.4161/mabs.2.3.11641
5.Baldo BA. Antibodies (Basel). 2022 Feb 25;11(1):17.
6.Song S, et al. J Immunol Res. 2016;2016:3072586.
7.Rispens T, et al. Nat Rev Immunol. 2023 Nov;23(11):763-778.Piseddu, I., et al., Gut, 2025. 74(9): p. 1528-1538.
9.Liu H, et al. Adv Ther. 2025 Sep;42(9):4611-4625
10.金蓓欣CSR数据
11.金蓓欣研究者手册
12.长春金赛药业有限责任公司. 金纳单抗GenSci048研究者手册
声明:
1.本材料旨在传递前沿信息和满足医疗卫生专业人士的医学信息需要,无意向您做任何产品的推广,不作为临床用药指导。
2.若您想了解具体疾病诊疗信息,请遵从医疗卫生专业人士的意见与指导。









